Ja, en "mengde maskiner" er på jobb i cellen
David Coppedge; 23. august 2022 Oversatt herfra
Bilde 1. topoisomerase2
 På samme måte som vi elsker de gamle standbyene (flagellum, cilium, ATP-syntase, etc.), bør vi aldri anta at saken for intelligent design er begrenset til de ikoniske favorittene. I 2002 hevdet Jed Macosko i Unlocking the Mystery of Life at det er "en rekke maskiner" på jobb i cellen - like mange som det er funksjoner som kroppen må utføre. Hver maskin er et vidunder av ingeniørkunst og presisjon. La oss besøke noen flere av dem.
På samme måte som vi elsker de gamle standbyene (flagellum, cilium, ATP-syntase, etc.), bør vi aldri anta at saken for intelligent design er begrenset til de ikoniske favorittene. I 2002 hevdet Jed Macosko i Unlocking the Mystery of Life at det er "en rekke maskiner" på jobb i cellen - like mange som det er funksjoner som kroppen må utføre. Hver maskin er et vidunder av ingeniørkunst og presisjon. La oss besøke noen flere av dem.
En annen topoisomerase
Discovery Institutes nylige animasjon av en type 2 topoisomerase blendet oss med dens evne til nøyaktig å kutte DNA og sy det sammen igjen for å fikse vridde løkker som kan sende et genom inn i et dødsspinn.
Video topoisomerase 2-lenke.
Familien av topoisomerasemaskiner inkluderer imidlertid seks typer like fantastiske. Topoisomerase 3β (forkortet TOP3B) mottok en ovasjon denne måneden fra Yang et al. i Nature Communications-lenke. Denne "regulerer R-loop-dynamikk og mRNA-oversettelse, som er avgjørende for genomstabilitet, nevroutvikling og normal aldring." TOP3B er en type 1 topoisomerase som reparerer en DNA-streng (se nedenfor for en enkel videodemonstrasjon).
Video topoisomerase 1 og 2 -lenke.
Detaljene er mer komplekse enn vist, som dette utdraget fra artikkelen demonstrerer:
-Som en type IA topoisomerase, virker TOP3B ved generell syre-base-katalyse for å bryte og gjenforene enkelttrådet DNA. Passering av en andre DNA-tråd gjennom det forbigående bruddet tillater spredning av hypernegativ DNA-supercoiling og katenering/knytting. I tillegg ble hsTOP3B nylig demonstrert som den humane RNA-topoisomerasen, nødvendig for normal nevroutvikling og foreslått å være et potensielt antiviralt mål ved RNA-virusinfeksjon. Her belyser vi de biokjemiske mekanismene til menneskelig TOP3B. Vi avgrenser rollene til toverdige metallioner, og til en konservert lysinrest (K10) i differensialkatalysen av DNA og RNA. Vi demonstrerer også at tre regulatoriske faktorer finjusterer den katalytiske ytelsen til TOP3B: TOP3B C-terminal halen, proteinpartneren TDRD3 og sekvensen til DNA/RNA-substratene.
Bilde 2. topoisomerase i arbeid

Som nevnt kan denne maskinen nøyaktig bryte og sammenføye enkeltstrenger av DNA for å løse opp knuter. I likhet med Type 2-motstykket som kan kutte og skjøte to tråder om gangen, fungerer TOP3B i en "tre-trinns strategi - DNA-spalting, trådpassasje, DNA-sammenføyning." Det krever tre finjusterte regulatoriske kofaktorer for å fungere. Og det er nødvendig for normal nevroutvikling.
En annen overraskelse er verdt å merke seg: Behovet for metallioner for å kutte nukleinsyrene: "tilsetning av Mg2+ og i større grad Mn2+ stimulerte DNA-binding og spaltning av TOP3B." Er det på sin plass å si at denne maskinen har et metallskjæreblad?
Nok et kastevåpen
Vi har lært om Type 3 Secretion System og Type 4 Secretion System i bakterier som skyter molekyler utenfor membranene sine, men det er en annen vi ikke har vurdert på en stund: Type 6. En Evolution News-artikkel i 2015 diskuterte dens avfyringsmekanisme . Nå har Lin Lin og kolleger ved University of Basel, Sveits, publisert en åpen artikkel i EMBO Journal som beskriver T6SS-montering. Maskinen ser ut som en kanon eller bazooka på figurene. Bemerkelsesverdig nok ser denne "store nanomaskinen som kan levere giftstoffer direkte over membraner til proksimale målceller" ut til å samle seg raskt ved kontakt når bakterien møter en rival i "interbakteriell konkurranse."
-Vi identifiserte en klasse med forskjellige, tidligere ukarakteriserte, periplasmatiske proteiner som kreves for denne dynamiske lokaliseringen av T6SS til celle-cellekontakt (TslA). Denne nøyaktige lokaliseringen er også avhengig av den ytre membranporin OmpA. Analysen vår kobler transmembran-kommunikasjon til nøyaktig timing og lokalisering av T6SS-montering, samt avdekker en vei som lar bakterieceller reagere på celle-celle-kontakt under interbakteriell konkurranse.
Dette innebærer at komponentene lagres lokalt i hele den indre membranen for å unngå kostnadene ved å opprettholde et arsenal over hele cellen. Det innebærer også kontaktsensorer for å aktivere sammenstillingen - som forfatterne fant.
-I dette arbeidet avslører vi en mekanisme for lokalisering av en kompleks nanomaskin som svar på kontakt med en annen celle. En slik presis posisjonering krever sannsynligvis tidsmessig og romlig koordinering av mange regulatoriske proteiner ved membranen. Siden mange T6SS-tilbehørproteiner forblir ukarakteriserte, foreslår vi at noen av disse proteinene kan være nødvendige for spatiotemporal regulering av T6SS-montering. Vi forventer at ytterligere mekanismer for dynamisk lokalisering av T6SS vil bli identifisert i flere bakterier og vise seg å spille en viktig rolle i deres patogenese eller økologi.
Forfatterne bruker strategiske oppdragsbegreper som 'angrep' i deres tro på at T6SS "sannsynligvis utviklet seg til å tillate effektivt drap av målceller." Men vi bør ikke ta krigføringsmotivet for alvorlig. De er bare bakterier. Kanskje er kolonien programmert til å regulere omgivelsene på denne måten. De forventer at bildebehandling med høyere oppløsning vil "avdekke ytterligere intrikate mekanismer for T6SS-målretting."
Nitrogenases svarte boks
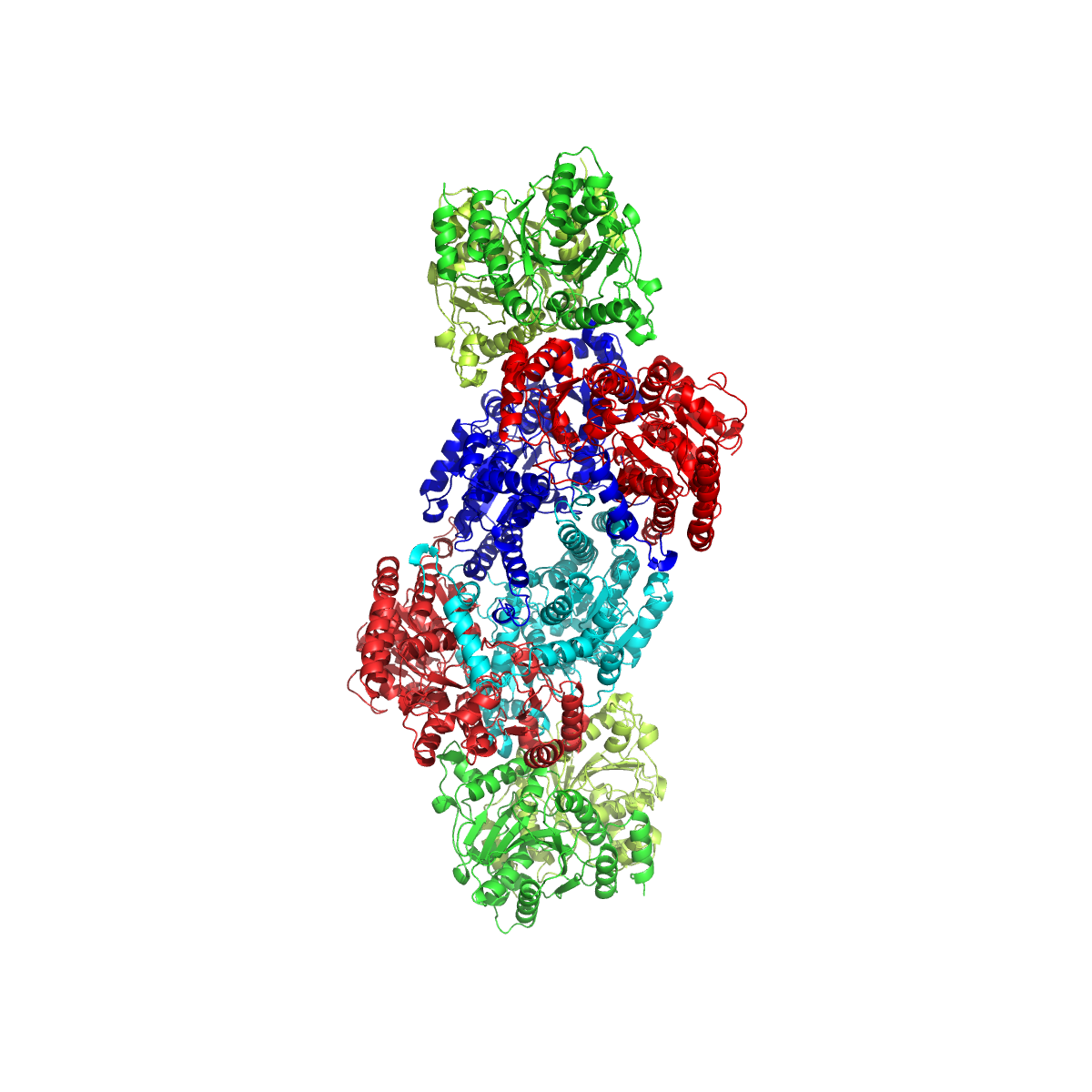 Et av de viktigste enzymene i hele naturen, nitrogenase har trosset analyse. Denne flerdelte maskinen med metaller i kjernen er det eneste enzymet som kan splitte de tøffe trippelbindingene til atmosfærisk nitrogen. Enzymet finnes kun i bakterier som danner symbiotiske forhold med røttene til enkelte planter. Biofysikere har i årevis prøvd å åpne den svarte boksen med nitrogenase, men dens konformasjonsendringer er flyktige og vanskelige å fange.
Et av de viktigste enzymene i hele naturen, nitrogenase har trosset analyse. Denne flerdelte maskinen med metaller i kjernen er det eneste enzymet som kan splitte de tøffe trippelbindingene til atmosfærisk nitrogen. Enzymet finnes kun i bakterier som danner symbiotiske forhold med røttene til enkelte planter. Biofysikere har i årevis prøvd å åpne den svarte boksen med nitrogenase, men dens konformasjonsendringer er flyktige og vanskelige å fange.
Bilde 4. Nitrogenase
-Reduserte former for nitrogen er avgjørende for biosyntesen av aminosyrer og nukleinsyrer, samt produksjon av gjødsel og mange kjemikalier. Som det eneste enzymet som er i stand til nitrogenfiksering, katalyserer nitrogenase åtte-elektronreduksjonen av atmosfærisk nitrogen (N2) og protoner (H+) til ammoniakk (NH3) og hydrogen (H2) (fig. 1A). Nitrogenase er et to-komponent enzym, som i sin vanligste form består av jernproteinet FeP (en γ2-homodimer) og molybden-jernproteinet MoFeP (en α2β2-heterotetramer) (fig. 1B) (4, 5). Nitrogenase er forskjellig fra de fleste redoksenzymer i kravet til adenosintrifosfat (ATP) hydrolyse for å muliggjøre suksessiv overføring av elektroner og protoner for substratreduksjon
Hannah L. Rutledge ved UC San Diego (Science) brukte kryo-elektronmikroskopi og rikelig med ATP for å fange noen flere bilder i 'filmen' til denne bemerkelsesverdige og unike maskinen. Basert på tilstandene de var i stand til å fange, tror de at de ser hvordan spillet spilles:
-Gitt asymmetrien mellom FeMoco-ene i de to αβ-halvdelene, er det fristende å foreslå en 'ping-pong'-type mekanisme der kofaktorene fortsetter gjennom hvert av de åtte katalytiske trinnene på en vekslende måte. Dette scenariet vil tildele FeP en dobbel rolle: (i) å levere et elektron til en αβ-underenhet av MoFeP og (ii) å undertrykke FeP-binding til den motsatte αβ-underenheten mens den primer den for katalytiske transformasjoner gjennom langdistanseaktivering av elektron, H+ og/eller substrattilgangsveier til den distale FeMoco. Å fastslå om en slik mekanisme er operativ vil kreve fremtidige studier, men vårt nåværende arbeid illustrerer at det er mulig å karakterisere nitrogenase under omsetningsforhold ved hjelp av cryo-EM ved nær-atomær oppløsning, som representerer et kritisk skritt mot å forstå mekanismen til dette gåtefulle enzymet i full strukturell detalj.
Når den dagen kommer, kan det revolusjonere landbruket. En artikkel fra Tsinghua University Press (Phys.org) sier at "det er fortsatt sårt behov for store gjennombrudd" for å erstatte den energikrevende Haber-Bosch-prosessen som "avbryter planetens nitrogensyklus, varmer opp kloden og potensielt påvirker helsen til millioner." Å imitere måten cellene gjør det på, kan tillate forskere å fikse nitrogen ved omgivelsestemperaturer. Nitrogenase er en molekylær maskin å se på!
Rubisco geometri
Bilde 5: Rubisco

Et annet viktig enzym for biosfæren er Rubisco, som fikserer karbon for omdannelse til sukker. Emily Reeves skrev om hvordan det fungerer i fjor -lenke, så leserne henvises til den artikkelen for bakgrunn. En ny åpen artikkel i Nature Communications av Lauren Ann Metskas et al. legger til noen interessante detaljer om geometrien: Den danner et gitter inne i bittesmå geometriske kupler.
-Dette arrangementet bevarer bevegelsesfrihet og tilgjengelighet rundt det aktive Rubisco-stedet og bindingsstedene for to andre karboksysomproteiner, CsoSCA (en karbonsyreanhydrase) og den uordnede CsoS2, selv ved Rubisco-konsentrasjoner som overstiger 800 μM. Denne karakteriseringen av Rubisco-lasten inne i α-karboksysomet gir innsikt i balansen mellom orden og uorden i organisering av mikrorom.
Forskerteamet påpeker at mange prokaryoter deler maskinene sine i mikrorom som dette, i motsetning til tidligere antakelser om at enzymene bare flyter rundt i det indre. I likhet med cellens ytre membran begrenser et proteinholdig skall "selektivt passasje av viktige mellomprodukter og forbedrer katalyse på-målet."
Interessen for "mikro-seksjons bioengineering" har vokst de siste årene, sier forfatterne. Artikkelen viser elektron-mikrofotografier av noen av disse bemerkelsesverdige geometriske rommene med Rubisco-enzymene pent pakket inne, men 'overraskende' ikke i kontakt med skallet. "Det seksdobbelte gitteret kan derfor være en pakkemekanisme for å bevare funksjon ved konsentrasjoner som ellers kunne krystallisere eller hindre funksjon." Det gir mening med design.
-Mikro-seksjons bioengineering er et voksende felt, og denne polymerisasjons-baserte mekanismen for effektiv, funksjonell og kontrollert pakking av enzymer kan være nyttig for fremtidig oppdagelse og design i både CBs [karboksysomer] og andre mikrorom.
Nok en gang viser observasjon og forventning om design fra et ingeniørperspektiv seg fruktbart når det gjelder å åpne de svarte boksene i cellen og kikke på de urlignende bevegelige delene inni. Fremtiden ser lys ut for nanobioteknologi, og med den øker den globale menneskelige blomstringen. Intelligent design har vist seg å være "nyttig for fremtidig oppdagelse og design."
Bilde 6: David Coppedge

David Coppedge er en frilans vitenskapsreporter i Sør-California. Han har vært styremedlem i Illustra Media siden grunnleggelsen og fungerer som deres vitenskapskonsulent. Han jobbet ved NASAs Jet Propulsion Laboratory (JPL) i 14 år, på Cassini-oppdraget til Saturn, til han ble kastet ut i 2011 for å ha delt materiale om intelligent design, en diskriminerende handling som førte til en nasjonalt publisert rettssak i 2012. Discovery Institute støttet saken hans, men en ensom dommer dømte mot ham uten forklaring. En naturfotograf, friluftsmann og musiker, David har B.S. grader i realfagsutdanning og i fysikk og holder presentasjoner om ID og andre vitenskapelige emner.
Oversettelse og bilder ved Asbjørn E. Lund
 På samme måte som vi elsker de gamle standbyene (flagellum, cilium, ATP-syntase, etc.), bør vi aldri anta at saken for intelligent design er begrenset til de ikoniske favorittene. I 2002 hevdet Jed Macosko i Unlocking the Mystery of Life at det er "en rekke maskiner" på jobb i cellen - like mange som det er funksjoner som kroppen må utføre. Hver maskin er et vidunder av ingeniørkunst og presisjon. La oss besøke noen flere av dem.
På samme måte som vi elsker de gamle standbyene (flagellum, cilium, ATP-syntase, etc.), bør vi aldri anta at saken for intelligent design er begrenset til de ikoniske favorittene. I 2002 hevdet Jed Macosko i Unlocking the Mystery of Life at det er "en rekke maskiner" på jobb i cellen - like mange som det er funksjoner som kroppen må utføre. Hver maskin er et vidunder av ingeniørkunst og presisjon. La oss besøke noen flere av dem.
 Et av de viktigste enzymene i hele naturen, nitrogenase har trosset analyse. Denne flerdelte maskinen med metaller i kjernen er det eneste enzymet som kan splitte de tøffe trippelbindingene til atmosfærisk nitrogen. Enzymet finnes kun i bakterier som danner symbiotiske forhold med røttene til enkelte planter. Biofysikere har i årevis prøvd å åpne den svarte boksen med nitrogenase, men dens konformasjonsendringer er flyktige og vanskelige å fange.
Et av de viktigste enzymene i hele naturen, nitrogenase har trosset analyse. Denne flerdelte maskinen med metaller i kjernen er det eneste enzymet som kan splitte de tøffe trippelbindingene til atmosfærisk nitrogen. Enzymet finnes kun i bakterier som danner symbiotiske forhold med røttene til enkelte planter. Biofysikere har i årevis prøvd å åpne den svarte boksen med nitrogenase, men dens konformasjonsendringer er flyktige og vanskelige å fange.
